ऊष्मागतिकी का तृतीय नियम |ऊष्मागतिकी के तृतीय नियम का अप्राप्ति कथन | Third Law of Thermodynamics in Hindi
ऊष्मागतिकी का तृतीय नियम (Third Law of Thermodynamics in Hindi)
ऊष्मा
गतिकी का तृतीय नियम (
ऊष्मा
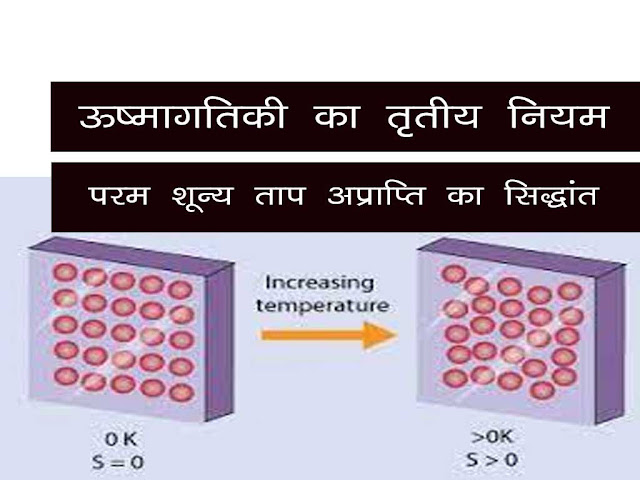
गतिकी के तृतीय नियम के अनुसार "किसी पदार्थ या निकाय (System) के तापमान को परमशून्य (Absolute zero) तक नहीं घटाया जा सकता।" अर्थात्
परम शून्य ताप एक आदर्श परिकल्पना (Ideal Hypothesis) या चरम अवस्था (Extream state) है
जिसे किसी भी विधि से प्राप्त करना असंभव है।
ज्ञातव्य है निम्नतापिकी (Cryogenics) द्वारा 107 'केल्विन तक का निम्न ताप प्राप्त किया जा चुका है जो कि 8 परम शून्य ताप (Zero Kelvin) के काफी निकट है।
ऊष्मागतिकी के तृतीय नियम से संबधित दैनिक जीवन के प्रश्न
क्या फ्रिज का दरवाजा खोल कर कमरे का ताप कम किया जा सकता है ?
- नहीं! उल्टा कमरे का तापमान और बढ़ जायेगा।
बंद कमरे में पंखा चलाने से कमरे के तापमान पर क्या प्रभाव पड़ता है।
- तापमान बढ़ जाता है। (क्योंकि पंखा चलाने से हवा के कण तेज गति करते हैं जिससे उनमें घर्षण बल बढ़ जाता है और ऊष्मा उत्पन्न होती है जो कमरे का ताप बढ़ा देती है।)
पंखा चलाने से कमरे का ताप बढ़ जाता है तो फिर शरीर को ठंडक का आभास क्यों होता है?
- क्योंकि पंखा चलाने से हवा की गति बढ़ जाती है, फलस्वरूप शरीर से निकले पसीने (Sweat) की वाष्पन दर भी बढ़ जाती है जिससे ठंडक का आभास होता है।
गर्म जल का फुहारा करने पर पानी ठंडा क्यों लगता है ?
- क्योंकि फुहारा (Fountain) बनने पर जल का पृष्ठीय क्षेत्रफल कई गुना बढ़ जाता है। ऐसा करने के लिए निकाय द्वारा वाह्य दाब के विरुद्ध कार्य करना पड़ता है जिसके लिए ऊर्जा, जल की आंतरिक ऊर्जा से ही प्राप्त होती है। साथ ही पृष्ठीय क्षेत्रफल बढ़ने से | वाप्पन भी बहुत तीव्र गति से होता है। इन दोनों ही कारणों से फुहारे की बूँदों का ताप कम हो जाता है।
परम शून्य ताप अप्राप्ति (unattainability) का सिद्धान्त या ऊष्मागतिकी के तृतीय नियम का अप्राप्ति कथन
- जूल-केल्विन प्रभाव का उपयोग 5K ताप के नीचे ताप पर द्रव हीलियम (liquid He) प्राप्त करने के लिए किया जा सकता है। द्रव हीलियम का तीव्र गति से रुद्घोष्म वाष्पन (adiabatic vaporisation) के परिणामस्वरूप ताप में और कमी होती है जो कि 4He के लिए 1K तथा 3He के लिए 0.3K होता है।
- मैग्नेटोकैलोरिक (magnetocaloric) प्रभाव के उपयोग से अनुचुम्बकीय (Paramagnetic) यौगिकों के ताप को लगभग 0.001K तक कम किया जा सकता है। सैद्धान्तिक रूप से, इस मैग्नेटोकैलोरिक प्रभाव को बार-बार उपयोग कर इससे भी कम ताप (0.001 K से कम ताप) उत्पन्न करने के लिये किया जा सकता है।
- हालांकि यह पाया गया कि द्रव जितना ज्यादा ठण्डा होता है, वाष्प दाब का मान कम होता जाता है जिससे द्रव को आगे वाष्प अलग कर (pumping) ठण्डा करना मुश्किल हो जाता है। अतः मैग्नेटोकैलोरिक प्रभाव में, यदि चुम्बकीय क्षेत्र में कमी करने पर ताप अपने प्रारम्भिक ताप T1 का 1/10 वें भाग (= TF1) हो जाता है तब उसी क्षेत्र में दूसरे बार कमी करने पर ताप TF2 हो जाता है जो कि ताप TF1 का दसवाँ भाग के बराबर होता है।
- इन परिस्थितियों में, चुम्बकीय क्षेत्र में इस प्रकार अनन्त बार कमी करने की आवश्यकता परम शून्य ताप प्राप्त करने के लिए होती है अर्थात् परम शून्य ताप (absolute zero temperature) की प्राप्ति के लिए इस चुम्बकीय क्षेत्र को अनन्त बार एकसमान कम करना चाहिए जो कि व्यवहार में सम्भव नहीं है। इस अनुभव पर आधारित एक व्यापक कथन निम्न है “कोई भी सीमित श्रेणी प्रक्रिया से परम शून्य ताप की प्राप्ति सम्भव नहीं है।
- इसे परम शून्य ताप अप्राप्ति (unattainability) का सिद्धान्त या ऊष्मागतिकी के तृतीय नियम का अप्राप्ति कथन (umattainability statement) कहते हैं। ऊष्मागतिको का तृतीय नियम एण्ट्रॉपी के शून्य हो जाने से संबंधित है। अर्थात् पूर्णत: व्यवस्थित निकाय (perfect ordered system) से ।
- ऊष्मागतिको के द्वितीय नियम के समान ही समतुल्य या क्रमागत कथन ऊष्मागतिकी के तृतीय नियम के बारे में दिया गया है।
चुम्बकीय क्षेत्र (H) के उत्क्रमणीय समतापीय वृद्धि के दौरान अणुचुम्बकीय नमक की एण्ट्रॉपी परिवर्तन में परिवर्तन होने के साथ ही ताप में कमी से एण्ट्रॉपी परिवर्तन में कमी होती है क्योंकि
ऊष्मागतिकी के तृतीय नियम का नसर्ट साइमन कथन
"किसी संघनित निकाय के उत्क्रमणीय समतापीय प्रक्रम में एण्ट्रॉपी परिवर्तन शून्य की और अग्रसर होता है, ज्यों-ज्यों तापमान शून्य की ओर बढ़ता है।" इसे ऊष्मागतिकी के तृतीय नियम का नसर्ट साइमन कथन (Nerst-simon statement) कहते हैं।
बहुत से भौतिक तथा रासायनिक तथ्य ऐसे हैं जो ऊष्मागतिकी के तृतीय नियम को सिद्ध करते हैं। उदाहरण के लिए, क्लोसियस फ्लेपरॉन समीकरण के अनुसार,
क्योंकि प्रथम कोटि के अवस्था संक्रमण के लिए Vf-Vi का मान शून्य नहीं होता है।
साइमन (Simon) तथा स्वेनसन (Swenson) ने यह पाया कि ठोस 1He के लिए dP/dT का मान तेजी के साथ शून्य की ओर अग्रसर होता है।
ऊष्मागतिकी के तृतीय नियम का एक अन्य महत्वपूर्ण परिणाम यह है कि जैसे-जैसे T→0, सभी विशिष्ट ऊष्मायें शून्य की ओर अग्रसर होते हैं। नियत आयतन पर परिवर्तन से एण्ट्रॉपी में परिवर्तन को निम्न प्रकार से लिखा जा सकता है -
यदि हम सीमा T →0 लें तब तृतीय नियम यह कहता है कि उपर्युक्त समीकरण में समाकल सीमित (finite) होना चाहिए। इसके लिए आवश्यक है कि Cv शून्य की ओर अग्रसर होना चाहिए जब T→0, अन्यथा समाकल अपसरित होगा। इस गुण को प्रायोगिक रूप से नर्स्ट ने स्थापित किया था।
- अतः हमने देखा कि ऊष्मागतिकी के तृतीय नियमानुसार एण्ट्रॉपी में परिवर्तन शून्य की ओर अग्रसर होता है ज्यों-ज्यों T→ 0 होता है। हमने यह भी देखा कि क्यों परम शून्य ताप की प्राप्ति सम्भव नहीं है। परम शून्य ताप प्राप्ति किसी सीमित श्रेणी प्रक्रियाओं से सम्भव नहीं है।
Also Read....
ऊष्मागतिकी क्या है, ऊष्मागतिक निकाय, ऊष्मागतिक साम्य स्थित
ऊष्मागतिकी का द्वितीय नियम ऊष्मागतिकी का प्रथम नियम की कमियाँ





Post a Comment